A hiperplasia prostática benigna (HPB) pode ser definida como a hiperplasia da zona de transição da próstata, causando disfunção miccional. Tenta-se, hoje, substituir o consagrado termo “prostatismo” por “sintomas do trato urinário inferior” (LUTS – Lower Urinary Tract Syntoms), a fim de frisar que não são apenas características de hiperplasia prostática benigna, uma vez que podem ocorrer em outras enfermidades, como prostatites, câncer prostático, esclerose do colo vesical, estenose de uretra, bem como em doenças que também incidem no sexo feminino, como cistites e disfunções neurogênicas da bexiga.
ASPECTOS GERAIS
A próstata de um adulto apresenta quatro regiões distintas: zona central (cone glandular que circunda os ductos ejaculadores, com massa correspondendo a 20% do total), zona periférica (composta por tecido glandular com aproximadamente 70% da massa total e é a área preferencial de carcinoma e inflamações), zona de transição (que é o tecido da glândula que circunda a uretra e colabora com cerca de 2 % de seu estroma e é área exclusiva de desenvolvimento de HPB) e zona anterior (tecido fibromuscular, desprovido de glândulas, com até um terço da massa prostática).
No homem normal, o peso da próstata varia em torno de 20g. Quando há HPB, a glândula passa a crescer, em média, 4g por década.
As manifestações clínicas de HPB são oscilantes, com períodos de remissão e exacerbação espontânea dos sintomas. Diante disso, observa-se que o paciente, na maioria das vezes, busca atendimento médico apenas em momentos de exacerbação dos sintomas.
Evolução do aumento da próstata e diminuição da capacidade de esvaziamento da bexiga
Com a melhora cíclica do quadro, ou através de tratamento farmacológico efetivo, o paciente pode ter a falsa impressão de cura de sua doença, até que os sintomas novamente se manifestem ou se estabeleça um tratamento prolongado e definitivo. Pacientes com HPB têm oito vezes mais chance de desenvolver cálculos na bexiga, o que indica a associação de estase urinária, causada pela HPB, com a gênese de cálculos vesicais.
ETIOLOGIA
Os principais fatores etiológicos da HPB são determinados por fatores hormonais, podendo ser associados à própria evolução da glândula prostática no homem. A idade e presença de função testicular normalsão os dois fatores mais importantes no desenvolvimento de HPB. A doença não se desenvolve em homens castrados antes da puberdade. Apresenta progressão com a idade, a ponto de cerca de 50% dos homens apresentarem tais achados por volta da sexta década de vida. A incidência histológica de HPB aumenta progressivamente com a idade, mas não há um aumento proporcional na prevalência dos sintomas relacionados à doença.
A avaliação preventiva da próstata, tanto para câncer, como para HPB, é recomendada no homem a partir dos 45 anos de idade, com ou sem sintomas. Na presença de antecedentes familiares de câncer prostático, deverá ser iniciada aos 40 anos.
AVALIAÇÃO E DIAGNÓSTICO
Pacientes com idade igual ou superior a 45 anos e com sintomas sugestivos de obstrução infravesical devem ser pesquisados de maneira padronizada com história clínica, pesquisa de sintomas obstrutivos e/ou irritativos, aplicação do questionário para avaliação quantitativa dos sintomas (IPSS), exame físico e exames laboratoriais. Existem diretrizes obrigatórias, recomendáveis, opcionais e ocasionais para a avaliação diagnóstica.
Quando os paciente acorda duas vezes ou mais durante a noite para urinar, isso pode significar sintomas obstrutivos causados por Hiperplasia Prostática Benigna.
Nas diretrizes obrigatórias estão a história clínica (cujo interrogatório poderá revelar sintomas obstrutivos ou irritativos), o exame físico (toque retal) e exames laboratoriais (EQU, creatinina e PSA). As diretrizes recomendáveis incluem o IPSS, a urofluxometria e curva de pressão/fluxo, a ultra-sonografia do trato urinário, o resíduo urinário pós-miccional e a glicemia de jejum. As diretrizes opcionais incluem a uretrocistoscopia, uretrocistografia retrógrada/miccional e a urografia excretora. As diretrizes ocasionais não têm valor na avaliação da HPB, mas servem para DX diferencial de situações especiais como bexiga neurogênica e doenças da uretra. Estes constituem um estudo urodinâmico completo, incluindo: cistometria, perfil pressórico uretral, eletromiografia esfincteriana e vídeo-urodinâmica.
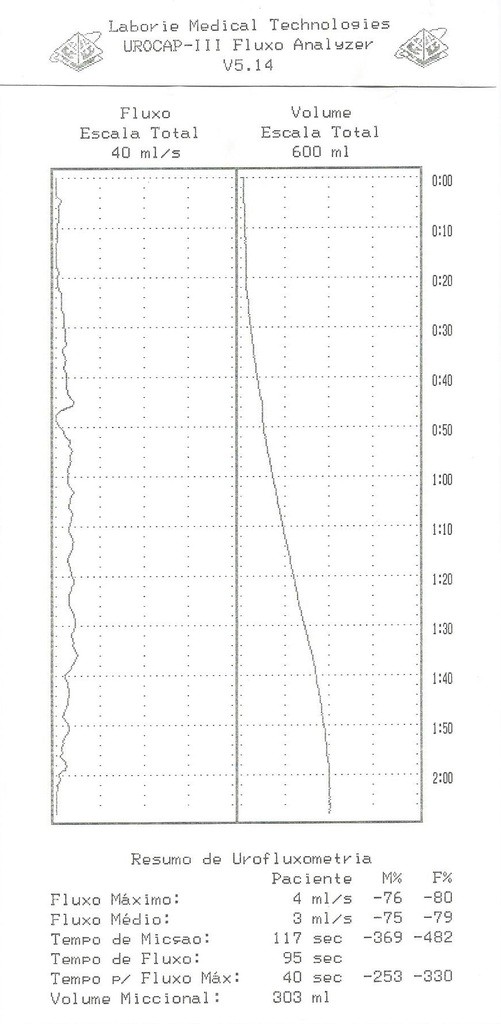
Este exame de Urofluxometria apresenta um gráfico com padrão obstrutivo, bastante comum em homens com Hiperplasia Prostática Benigna e obstrução urinária causada pela hiperplasia. Repare que o Pico de fluxo Máximo é de 4ml/s (Valor Normal: > 12ml/s).
SINTOMAS
A HPB causa aumento da resistência ao fluxo urinário infravesical, clinicamente determinado por:
a. sintomas obstrutivos (relacionados à obstrução mecânica ao fluxo urinário):
– jato fraco e/ou intermitente;
– hesitação miccional;
– esforço miccional;
– gotejamento pós-miccional;
– esvaziamento incompleto;
– incontinência paradoxal.
b. sintomas irritativos (relacionados aos efeitos secundários da obstrução crônica sobre o músculo detrusor):
– polaciúria;
– disúria;
– noctúria;
– urgência miccional;
– urgência-incontinência.
A intensidade desses sintomas pode ser quantificada subjetivamente, através de escores internacionais (como o IPSS), ou objetivamente, avaliando-se os sintomas através de urofluxométrica e curva pressão/fluxo.
Avaliação Quantitativa Dos Sintomas (IPSS): o International Prostatic Sympton Score é um questionário referente aos sintomas de prostatismo que é aplicado ao paciente para quantificar a intensidade de sintomas. Indica a necessidade de tratamento, mas não se presta como método diagnóstico, porque não é específico para diagnóstico de doença obstrutiva prostática. É o padrão mais utilizado para determinação da eficácia dos tratamentos clínicos realizados ou em andamento.
Escore Internacional de Sintomas Prostáticos – IPSS
| Nenhuma | Menos de 1 vez | Menos da metade das vezes | Metade das vezes | Mais da metade das vezes | Quase sempre | |
| 1. No último mês, quantas vezes você teve a sensação de não esvaziar completamente a bexiga após terminar de urinar? | 0 | 1 | 2 | 3 | 4 | 5 |
| 2. No último mês, quantas vezes você teve de urinar novamente em menos de 2 horas após ter urinado? | 0 | 1 | 2 | 3 | 4 | 5 |
| 3. No último mês, quantas vezes você observou que, ao urinar, parou e recomeçou várias vezes? | 0 | 1 | 2 | 3 | 4 | 5 |
| 4. No último mês, quantas vezes você observou que foi difícil conter a urina? | 0 | 1 | 2 | 3 | 4 | 5 |
| 5. No último mês, quantas vezes você notou que o jato urinário estava fraco? | 0 | 1 | 2 | 3 | 4 | 5 |
| 6. No último mês, quantas vezes você teve de fazer força para começar a urinar? | 0 | 1 | 2 | 3 | 4 | 5 |
| nenhuma | 1 vez | 2 vezes | 3 vezes | 4 vezes | 5 vezes | |
| 7. No último mês, quantas vezes, em média, você teve de se levantar à noite para urinar? | 0 | 1 | 2 | 3 | 4 | 5 |
Cada resposta pode variar de 0 a 5, dependendo da intensidade de cada sintoma, e, de acordo com a soma dos resultados obtidos, os pacientes podem ser classificados em:
– sintomatologia leve – de 0 a 7
– sintomatologia moderada – de 8 a 19
– sintomatologia grave – de 20 a 35
Posteriormente, foi introduzida uma nova pergunta para avaliar a qualidade de vida em função dos sintomas miccionais:
| Feliz | Muito satisfeito | Satisfeito | Regular | Insatisfeito | Muito insatisfeito | Infeliz | |
| Se você tivesse que passar o resto de sua vida com sua condição urinária da forma como está hoje, como se sentiria? | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
Sinais: a HPB pode se manifestar pelos sinais: jato fraco ou gotejamento (avalição clínica), hematúria, infecções do trato urinário (ITU) de repetição e retenção urinária aguda (dor suprapúbica + oligoanúria + globo vesical palpável).
Toque Retal: avalia as características do tecido prostático (volume, consistência, irregularidade, limites, sensibilidade e mobilidade). Sabe-se que o toque retal avalia qualitativamente apenas cerca de 60% do volume prostático. A grosso modo, uma polpa digital do examinador corresponde a 10g de peso prostático. O toque retal pode sugerir o diagnóstico de HPB pelo aumento de volume da próstata, entretanto é importante salientar que o volume prostático não está diretamente relacionado à intensidade dos sintomas.
Laboratório: devemos estar atentos para análise urinária (E.Q.U., urocultura, resíduos urinários), avaliação de função renal (creatinina e uréia) e PSA. Obstrução crônica por HPB pode der causa de IRA pós-renal.
PSA (antígeno prostático específico): é uma glicoproteína produzida quase que exclusivamente pelo tecido prostático, sendo de fundamental importância na avaliação da patologia prostática. Estima-se que 1g de tecido com HPB aumente o PSA em 0,3 ng/ml, enquanto que 1g de adenocarcinoma o eleva em 3 ng/ml. Níveis de PSA acima de 10 ng/ml indicam alta probabilidade de neoplasia, enquanto níveis abaixo de 4 ng/ml tornam a probabilidade de carcinoma muito pequena (menor que 20%). Sabe-se, também, que até 25% das HPBs têm PSA acima de 4 ng/ml. Quando o valor do PSA está entre 4 e 10 ng/ml, podemos utilizar a relação entre PSA livre e PSA conjugado. Além da HPB e do carcinoma de próstata, os níveis de PSA podem estar elevados em situações como: idade avançada em função do volume prostático, ejaculação recente, inflamação ou infecção prostática e trauma prostático (perineal) persistente.
Imagem: exames principalmente empregados na determinação do diagnóstico diferencial. A determinação de aumento do volume prostático pode sugerir HPB e, para tal, podemos dispor do toque retal e ultra-sonografia abdominal ou transretal. O ultra-som também pode ser útil na determinação de resíduo urinário. A urografia excretora (UIV) pode, em quadros avançados, demostrar uretero-hidronefrose bilateral e deformidades ureterais (ureter em gancho). A uretrocistografia retrógrada e miccional (UCRM) evidencia uma ¨bexiga de esforço¨, onde se observam espessamento de parede vesical, pseudodivertículos e um formato de “pinheiro de Natal”.
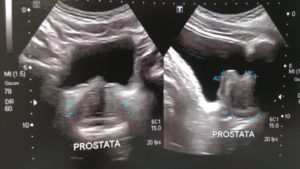
Exame de ultrassom calculando o volume prostático e mostrando o lobo mediano (crescimento da próstata para dentro da bexiga)
Endoscopia: a cistoscopia evidencia alterações anatômicas vesicais secundárias, como trabeculações, pseudodivertículos (detectadas por meio de cistoscopia em graus avançados da doença) e ¬ das zonas prostáticas peri-uretrais (lobos laterias e mediano). Também visualiza o tamanho da próstata (uretra supramontanal) e pode estimar seu grau de obstrução.
Urofluxometria: é recomendável no diagnóstico inicial, durante ou depois do tratamento, para determinar a eficácia terapêutica. Por ser um método não-invasivo e de importante valor clínico, deverá idealmente ser realizado antes de qualquer proposta terapêutica. Tal exame deverá ser realizado, no mínimo, 2 vezes e não tem valor quando o volume urinário for menor que 150 ml. Um fluxo urinário máximo (Qmáx.) abaixo de 15 ml/s é sugestivo de obstrução.
DIAGNÓSTICO DIFERENCIAL
1. Bexiga neurogênica: a instabilidade ou hiperreflexia detrusora simula síndrome semelhante – pesquisar achados neurológicos, lembrar que a obstrução crônica também pode ser causa de instabilidade.
2. Estenose de uretra: história de trauma ou uretrites (DST) – importante avaliação endoscópica ou UCRM.
3. Adenocarcinoma de próstata: pode ser causa de obstrução vesical – análise do toque retal (próstata endurecida ou com nódulo) e PSA (> 4); se houver dúvida, realizar biópsia prostática, preferencialmente guiada por ultra-sonografia transretal.
4. Prostatite aguda: pode ser causa de obstrução de retenção urinária aguda – pesquisar quadro infeccioso (febre, dor perineal), leucograma, EQU e urocultura.
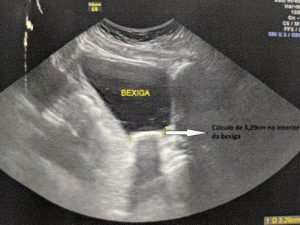
5. Cálculo de bexiga: sintomas obstrutivos, urina tranca subitamente durante micção, hematúria, disúria – pode ser conseqüência de obstrução urinária (por hiperplasia prostática ou estenose de uretra), resíduo urinário elevado ou ITU (Infecções do trato Urinário).
6. ITU: determina sintomas principalmente irritativos – pcte com E.Q.U. alterado e urocultura positiva.
TRATAMENTO CLÍNICO
Indicado para pacientes com sintomas leves a moderados (IPSS < 18 ou urofluxometria com fluxo máximo > 11 ml/s).
Drogas
– Fitoterápicos: poucos efeitos adversos, mas com resultados duvidosos.
– Alfa-Bloqueadores: (doxazosina, terazosina, tamsulozina, alfazosina): provocam relaxamento do arcabouço prostático fibromuscular e colo vesical, com resposta objetiva e rápida em próstatas de pequeno volume (20 a 40 g) e obstrução de lobos laterais.
– Anti-androgênicos: (finasterida): bloqueiam a conversão de testosterona em DHT, reduzindo o volume prostático e sintomas; resposta satisfatória a longo prazo (melhora dos sintomas em 2-3 meses de tto) e em próstatas de grande volume (> 50 g). Os principais efeitos adversos são disfunção erétil (em menos de 10% dos pctes) e diminuição do volume ejaculado.
TRATAMENTO CIRÚRGICO
Indicações de cirurgia para pacientes com:
– sintomas severos (IPSS > 25 ou urofluxometria com fluxo máximo < 10 ml/s);
– prejuízo ou ameaça à função renal;
– hematúria persistente de causa prostática;
– ITU repetição;
– retenção urinária aguda;
– urolitíase.
Os principais riscos dos tratamentos cirúrgicos são a incontinência urinária e a ejaculação retrógrada.
TÉCNICAS CIRÚRGICAS MINIMAMENTE INVASIVAS
Ressecção Trans-Uretral (RTU) de próstata: ideal para próstatas de volumes inferiores a 50g, rápida recuperação pós-operatória e pequeno período de internação hospitalar.
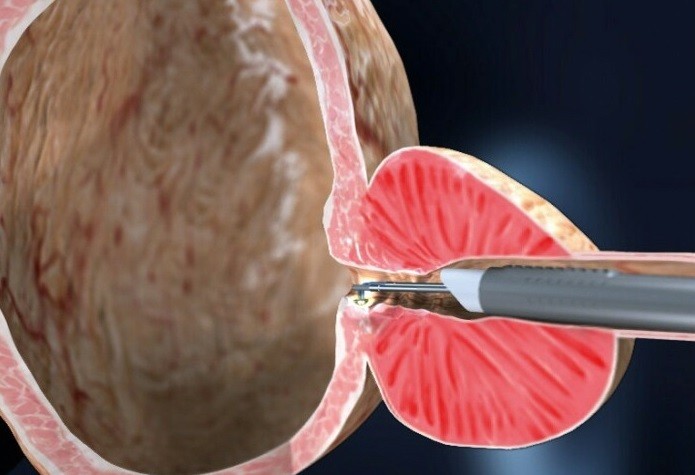 |
| Esquema demonstra a bexiga no lado esquerdo e a alça de ressecção na loja prostática… |
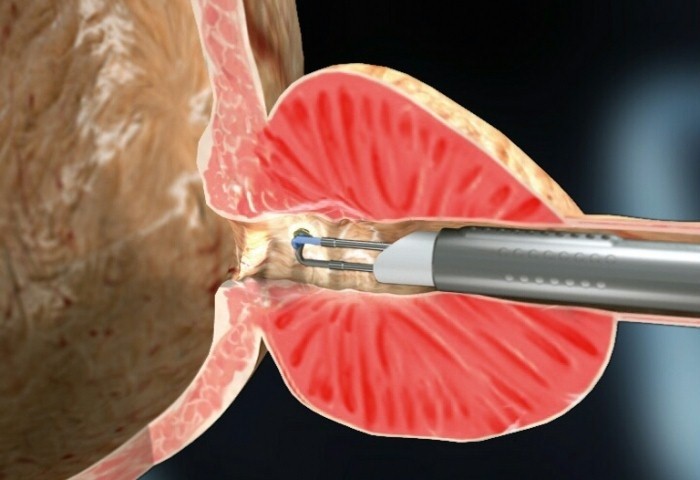 |
| …início da ressecção… |
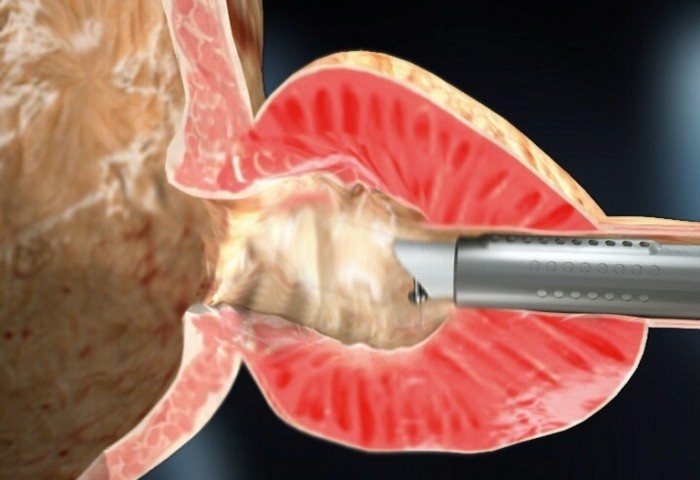 |
| … término da ressecção: loja prostática aberta… |
 |
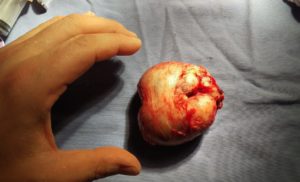
| fragmentos retirados no final da RTU de próstata que serão submetidos a exame anátomo-patológico. |
- Termoterapia transuretral de microondas (TUMT)
Esta técnica usa o calor das microondas para destruir o excesso de tecido da próstata. As microondas são enviadas pela uretra através de um cateter. Um computador é usado para controlar as microondas e a quantidade de calor que elas emitem. Há também um sistema de arrefecimento no lugar para proteger o trato urinário de danos.
TUMT geralmente pode ser concluída em uma hora em um ambulatório configuração. Muitas vezes, os pacientes não precisam de anestesia.
- Ablação com agulha transuretral (TUNA).
Tal como o TUMT, este procedimento também utiliza calor para destruir o excesso de tecido prostático. No entanto, o calor vem na forma de ondas de rádio que são entregues através de agulhas. Shields são usados para proteger o trato urinário. Geralmente, os procedimentos TUMT duram uma hora ou menos e são feitos em regime ambulatorial. Os pacientes recebem anestesia local. Alguns homens sentem uma sensação de queimação durante o procedimento.
- Termoterapia induzida pela água.
Com esta técnica, o cirurgião utiliza um cateter especial que forma um balão no centro da próstata. A água aquecida é enviada para baixo do cateter para encher o balão. Como TUMT e TUNA, o calor destrói o tecido. A temperatura da água é regulada por um computador, de modo que a uretra e a bexiga são protegidas.
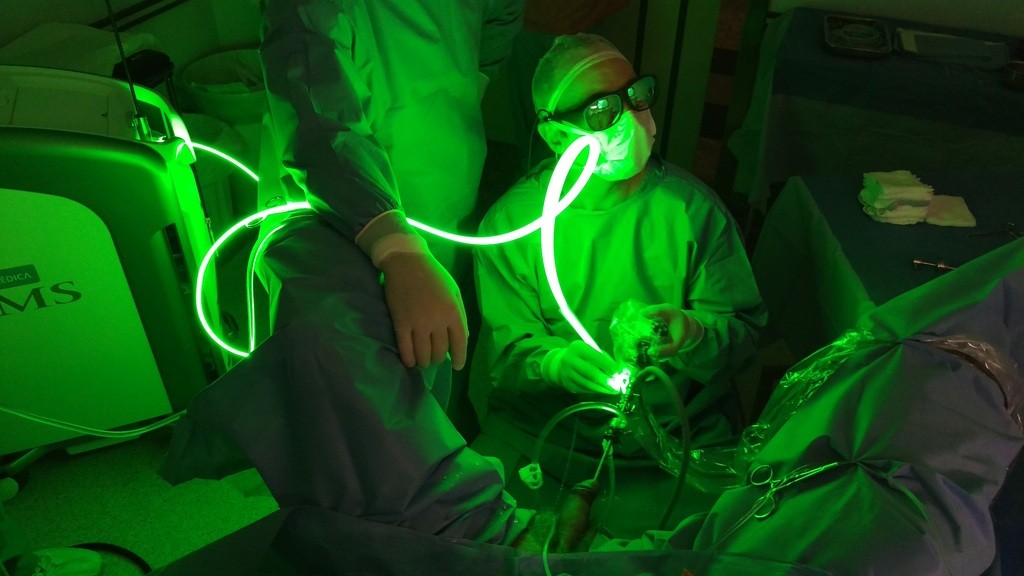
- Vaporização Prostática com Laser.
O tecido prostático não é ressecado nem retirado ao final do procedimento. O adenoma (hiperplasia prostática benigna) é vaporizado com a energia do laser. O procedimento é semelhante à RTU, porém apresenta risco menor de sangramento e retirada mais precoce da sonda uretral no pós operatório. Este procedimento pode ser realizado em pacientes anticoagulados ou que fazem uso de antiagregantes plaquetário (AAS, clopidogrel).
Curso teórico-prático com simulador de atualizações da técnica cirúrgica do Greenlight Laser no Congresso Americano de Urologia – AUA Boston 05/2017.
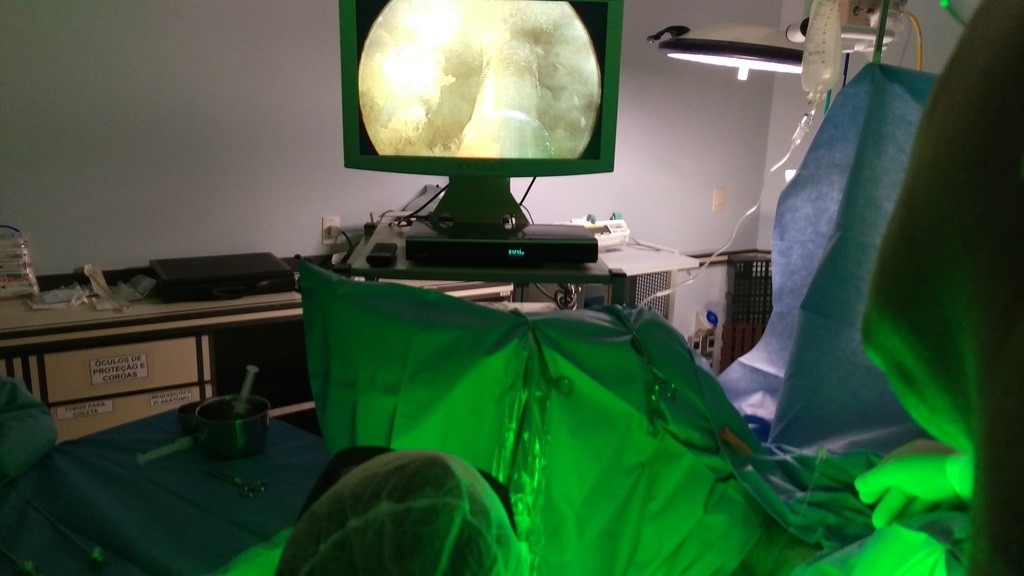
O vídeo abaixo demonstra uma vaporização de tecido prostático hiperplásico benigno. A cirurgia endoscópica foi realizada pelo Dr. Alessandro Rossol no Hospital Mãe de Deus, de Porto Alegre, RS, Brasil. O paciente havia apresentado uma retenção urinária aguda após hospitalização por infarto agudo do miocárdio. Devido ao uso de anticoagulante oral, teve contra-indicada a realização da tradicional RTU-P (Ressecção Transuretral da Próstata). O tratamento com laser foi a forma mais segura de desobstruir a via urinária, permitindo ao paciente voltar a urinar espontaneamente, sem o uso de sonda.
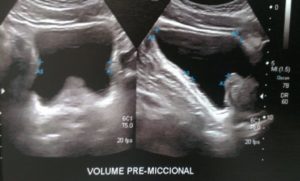
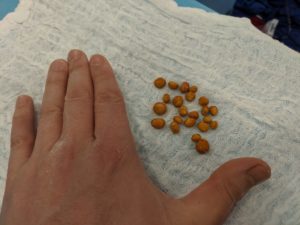
Nas imagens abaixo apresentamos um caso de um paciente com hiperplasia prostática benigna com obstrução severa e inúmeros cálculos dentro da bexiga.
O paciente oi submetido, no mesmo ato cirúrgico, à retirada endoscópica transuretral dos cálculos e, também, à vaporização da próstata com greenlight laser.
- Stenting é outro tipo de procedimento minimamente invasivo, mas não envolve a remoção de tecido da próstata. Em vez disso, stents – pequenas bobinas ou molas feitas de plástico ou metal – são inseridos na uretra para mantê-lo aberto. Stenting requer anestesia local ou espinhal e pode ser feito em um ambiente ambulatorial. Não é comum, entretanto, e é reservado geralmente para os homens que são pacientes de alto risco para outros tratamentos cirúrgicos de BPH / LUTS.
TÉCNICA CIRÚRGICA TRADICIONAL OU ABERTA
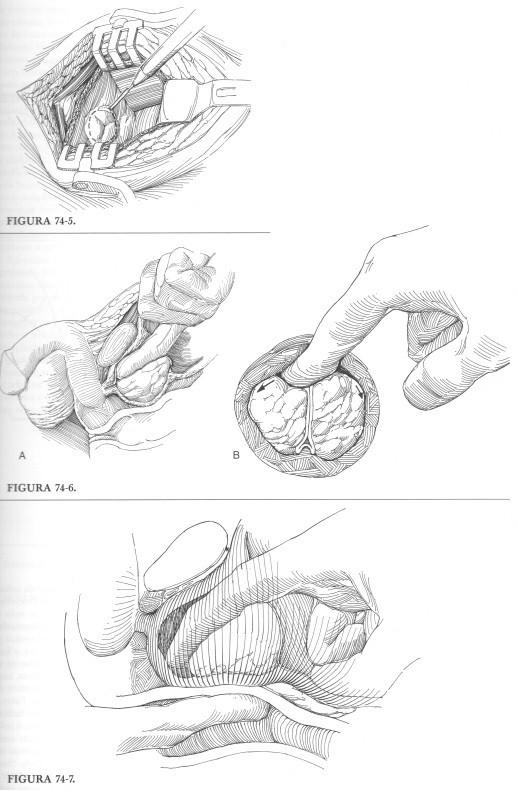
Prostatectomia Simples ou Adenomectomia: pode ser realizada por via retropúbica ou transvesical; ideal para próstatas de volume superior a 50g, por diminuir o risco de síndromes de absorção hídrica com sangramentos e IRA (Insuficiência Renal Aguda).
As figuras acima demonstram uma prostatectomia simples transvesical realizada por técnica aberta para retirada de um anenoma prostático em paciente com sintomas prostáticos obstrutivos e hiperplasia prostática benigna.
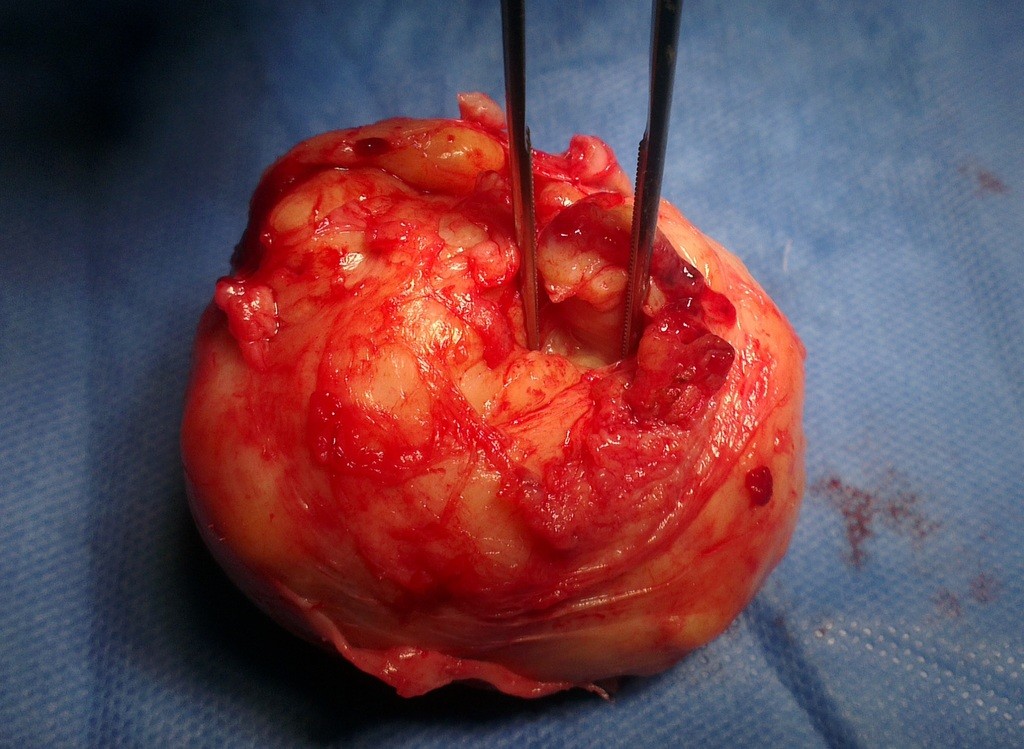
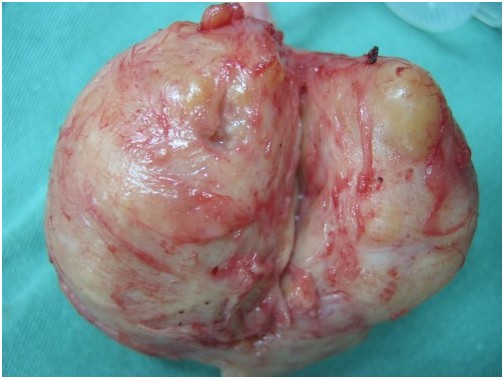
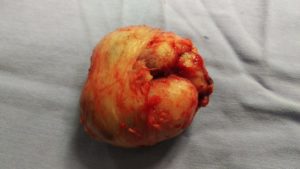
Adenoma prostático pesando 150 gramas em Prostatectomia Simples (Adenomectomia)
Fonte Bibliográfica:
Campbell-Walsh: Tratado de Urologia, 9a.
‘Revisão e Testes em Cirurgia‘: Alessandro Rossol e cols – 1.ed.- Porto Alegre, Editora Livre, 2004 / ISBN 85-98551-01-5.
Urologia Fundamental, 2010 – Sociedade Brasileira de Urologia.
Hinmann: Atlas de Cirurgia Urológica, 2010.
Fotografias e Vídeo:
Arquivo pessoal – Dr. Alessandro Rossol






0 resposta
Existe algum procedimento cirúrgico p/Hiperplasia Benigna que dispensa internação hospitalar, ou seja, Acabou a cirurgia vai p/casa.?
Todos os procedimentos cirúrgicos para tratamento de HBP (Hiperplasia Benigna Prostática) necessitam internação hospitalar. Na RTU-p (Ressecção Transuretral Prostática), onde a fonte de energia é o eletrocautério, devido ao sangramento habitual nos dias de pós-operatório com sondagem e irrigação da loja prostática com soro fisiológico, o paciente fica hospitalizado entre 3 e 6 dias. Na prostatectomia aberta simples (adenomectomia) o paciente também permanece hospitalizado por um período semelhante ao da RTU-p. Com o Greenlight laser, normalmente o paciente realiza a cirurgia num dia e recebe alta no dia seguinte. Eventualmente poderá ficar mais um ou dois dias hospitalizado.
Antigamente existia um procedimento para colocação de um dispositivo chamado de Urolume, que era de caráter ambulatorial, com alta no mesmo dia. Entretanto devido aos maus resultados, principalmente ao deslocamento deste “expansor” da loja prostática, hoje em dia não se tem mais utilizado esta técnica.